小児心臓学の分野で国内で最も革新的な研究者を擁するチルドレンズ ハート センターは、地域社会および世界中で心臓病を患う子供たちの健康と福祉を変革しています。
ドフ・マケルヒニー医学博士
スタンフォード大学ルシール・パッカード小児病院小児心臓センター臨床・トランスレーショナルリサーチプログラムディレクター
もし、患者が様々な診療所や病院で収集した医師の記録、MRI、X線写真、検査結果をすべて一元管理できたらどうなるでしょうか? 大規模データを分析することで、医師や研究者はどのような洞察やパターンを発見できるでしょうか?
スタンフォード大学医学部の心臓胸部外科教授であるドフ・マケルヒニー医学博士は、そのようなつながりのある世界における患者ケアがどのようなものになるかを探る研究の進歩を推進しています。
マケルヒニー氏が説明するように、電子患者データとデータ収集デバイスはますます普及しており、ハイスループット分析を活用して重要な知見を引き出し、より正確で個別化された効果的な医療を実現する絶好の機会が生まれています。こうした進歩は、単心室性心疾患の小児など、複雑で慢性的な疾患を抱える最も脆弱な患者にとって特に重要です。
1年前、マケルヒニー氏はスタンフォード大学に移り、小児心臓センターの新たな臨床・トランスレーショナル・リサーチ・プログラムの責任者に就任しました。この革新的なプログラムは、全米でも数少ないプログラムの一つであり、ルシール・パッカード小児病院スタンフォード校における小児心臓研究の共同研究に不可欠な基盤を提供し、臨床医と研究者を結集することで、基礎科学の知見を医療の進歩につなげるプロセスを加速させています。
マッケルヒニー氏はこれらの共同研究を通して、新たな研究分野の開拓に熱心に取り組んでいます。「先天性心疾患を持つ小児および成人の治療は飛躍的な進歩を遂げてきましたが、未解決の問題やこの分野を前進させる機会は依然として数多く残されています」と彼は指摘します。
臨床およびトランスレーショナル研究プログラムでは、患者の基本的な病態生理学、評価、ケアの調査、新しい医療機器および技術の開発、ビッグデータの使用による患者記録の情報の分析、複雑な臨床および病理学的プロセスの理解の深化に取り組んでいます。
マケルヒニー氏は、個別化医療を心臓治療にどのように応用できるかを解明することを目指しています。「腫瘍専門医は遺伝子変異の種類に応じて異なる薬剤を使用し、それによって異なる治療が可能になります」と彼は言います。「先天性心疾患でも同じことが言えるかもしれません。患者をより明確かつ詳細に理解することで、よりきめ細かな治療が可能になるかもしれません。」マケルヒニー氏が先天性心疾患の有望な治療法として研究に熱心に取り組んでいるもう一つの分野は、幹細胞療法です。これは、患者一人ひとりのニーズに合わせて個別化できる治療法です。
幸いなことに、マケルヒニーはこれらの重要な疑問への答えを見つけるのに最適な場所にいます。臨床・トランスレーショナル・リサーチ・プログラムは、ビッグデータを活用してバイオメディシンの課題に取り組み、疾患の診断、治療、予防に世界的な影響を与える研究集約型の大学であるスタンフォード大学という理想的な立地にあります。
「スタンフォードには、情報を創造的かつ進歩的な方法で扱うという点で、ダイナミックで革新的な文化があります」とマケルヒニー氏は言います。「私たちは、その文化を活かして、心臓病プログラムでユニークな取り組みをしたいと考えています。私たちはまさに順調に進み、多くの人々を結びつけています。」
マケルヒニー氏は、小児心臓病専門医が扱う解剖学的・生理学的複雑さを考慮すると、依然として解決すべき課題が山積している点が、小児心臓病学の魅力の一つだと語る。「多方面にわたって、学ぶべきことがたくさんあります。私がこの仕事を始めた頃とは全く違う仕事です」と彼は言う。「10年後も同じではないでしょう。」
アリソン・マースデン博士
小児科(心臓病学)およびバイオエンジニアリングの准教授
10年前、アリソン・マースデン博士は、より静かな航空機の翼を設計していました。しかし、スタンフォード大学で機械工学の博士号を取得するため、翼の最適化に関する論文を書き終えた時、彼女は博士研究員として、より現実的な研究分野を追求したいと考えるようになりました。
結局のところ、彼女の機械工学と航空宇宙工学のバックグラウンドは、先天性心疾患を持つ子供たちのためのより良い手術を設計するという現在の役割に最適な基盤を提供しました。
「もっと人間的な応用が可能な研究に興味があったんです」と彼女は言います。「そして、子どもたちの医学的問題に取り組むことは、非常にやりがいのあることだと感じました。」
マースデンは、スタンフォード大学の小児心臓専門医でありダンレヴィファミリー小児科(心臓病学)教授でもあるジェフリー・ファインスタイン医学博士(公衆衛生学修士)と協力し、心臓病学について学び、ルシール・パッカード小児病院でのファインスタインの回診に同行することに長い時間を費やした。
スタンフォード大学に通っていた頃のことです。「まるで医学生のように質問攻めにされました」とマースデンさんは笑いながら振り返ります。
最終的に、マースデンとファインスタインは主要な協力者となった。
カリフォルニア大学サンディエゴ校で数年間教鞭を執った後、最近スタンフォード大学に戻り、小児科心臓病学の准教授となったマースデン氏は、流体力学の知識を応用し、先天性心疾患を持つ子どもたちの心臓や血管における血液の流れを解明しています。彼女はコンピュータシミュレーションを診断に活用することから始め、現在では手術手順の改善策の探求にもコンピュータモデルを活用しています。
医療問題に対する工学的ソリューションを構築するチームワークは比較的一般的だとファインスタイン氏は説明する。しかし、マースデン氏のように、そうした理論的な設計が臨床現場で機能することを保証するのは、乗り越えるべきハードルが高い。「マースデン氏のような仕事を選び、彼女と同じくらい優れた成果を上げているのは、ごく少数の人たちです」とファインスタイン氏は言う。「患者ケアをさらに向上させていく上で、彼女を小児心臓学の教員として迎えることは、非常に大きな財産です。」
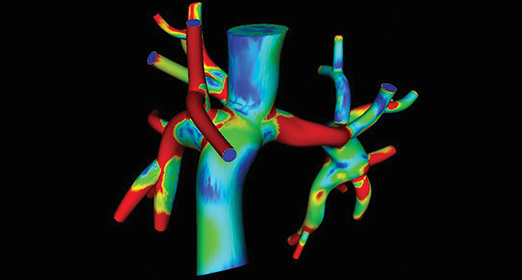
マースデン氏の研究は、新しい手術設計を患者に試す前にコンピュータ上でテストする方法を提供する。これは、エンジニアがコンピュータコードを用いて飛行機や自動車の新しい設計をテストするのと似ている。マースデン氏と彼女のチームは、フォンタン手術と呼ばれる手術法の改良版をシミュレーションした。フォンタン手術は、単心室欠損症の子どもたちが生存するために受けなければならない一連の手術の最終段階である。
フォンタン手術では、体から心臓へ血液を戻す太い静脈を、酸素化されていない血液を肺へ送る動脈に直接接続し、T字型の接合部を形成します。これにより心臓を片側からバイパスし、循環によって単一のポンプ室が最適に活用されます。マースデン氏はMRI画像データから得られたモデルを用いて、フォンタン手術用のY字型の新しい接合部(Yグラフトフォンタン)をコンピュータモデルで設計・最適化しました。コンピュータモデルは、小児外科医がこの手術が患者に有益かどうか、また患者の心臓が中程度の運動時にどのように機能するかを判断するのに役立ちます。
「コンピューターモデリングによって、ハイリスク・ハイリターンのアプローチをテストすることが可能になります」とマースデン氏は言う。「患者にリスクを与えることなく、斬新なアイデアをテストできるのです。」
このY字型グラフトの改良は、最近6人の患者を対象としたパイロットスタディで成功し、有望な臨床結果が得られました。マースデン博士は現在、他の小児心臓手術にも応用できる改良と新たなアプローチの開発に着手しています。
「アリソンの研究のおかげで、他の方法では見ることのできないものを見ることができるようになりました」とファインスタイン氏は語る。「シミュレーションに基づく医療という概念自体が、患者にリスクを全く与えずに様々なことを試す機会を与えてくれます。この種のコンピューターモデリングを使えば、実際に患者に試す前に100回ものシミュレーションを行うことができます。」
スシュマ・レディ医学博士
小児科(心臓病学)助教授
マウスのRNAの微細な鎖から、先天性心疾患を持つ子どもたちがより長く、より健康に生きられるようになる方法を学べるでしょうか?小児科心臓病学助教授のスシュマ・レディ医学博士は、その可能性を示唆し、マウスの血液中に、心不全の兆候を医師に警告できるシグナルを発見しています。
レディ氏が心臓病学に興味を持ったのは医学生時代でした。なぜ心臓病学を選んだのか?「この分野は生理学的な面白さがあり、臨機応変に考えさせられるからです」とレディ氏は言います。それ以来、先天性心疾患の治療は飛躍的に進歩し、患者さんは20年前よりも生存し、より良い状態を保っています。
「私たちは患者さんを助けるために、技術の限界を押し広げ続けています」と彼女は言い、まだ多くの疑問が未解決のままであることを指摘した。
レディ氏は特に、片方の心室が機能している状態で生まれた子どもたち、いわゆる単心室性心疾患に関心を寄せています。この状態を改善するために一連の複雑な手術を行った後も、これらの子どもたちは心臓のポンプ機能が2つではなく1つしかなく、そのため正常な心臓を持つ子どもたちほど強くありません。
「いずれ、これらの子供たちは皆、心不全に陥ります。全員が」とレディ氏は説明する。医師は心エコー図や心臓MRIを用いて、これらの患者の心臓の状態を把握するが、これらの画像診断技術では、問題の初期兆候を検出できない場合もある。心不全の臨床的証拠が現れる頃には、病状は進行しており、ほとんどの治療法ではこのプロセスを逆転させることができない。
レディ氏は、ヒトの先天性心疾患患者に見られる症状を模倣したマウスの心臓欠陥を研究することで、この問題に取り組んでいます。具体的には、心不全を引き起こす遺伝子やタンパク質を制御する機構を研究しています。彼女は、極小のRNA鎖、すなわちマイクロRNAが、心不全の兆候の一つであることを発見しました。「私たちは、重要だと考えられるマイクロRNA群を特定しました」とレディ氏は言います。「これらのマイクロRNAは、心臓の代償不全が始まった時期を、現在の方法よりもはるかに早く知らせてくれます。心臓病の小児における初期データでは、これらのバイオマーカーが疾患進行の有用な予測因子であることが示されています。」
彼女は現在、他の研究機関と共同で、マウスで特定した血液バイオマーカーが、より大規模なスケールで小児にも存在するかどうかを調べています。彼女によると、最良のアプローチは、血液バイオマーカー検査と既存の画像検査を組み合わせることで、先天性心疾患の患者の状態を最も包括的に把握することだそうです。
レディ氏の研究は最近、米国国立衛生研究所(NIH)のK08助成金であるメンター付き臨床科学者研究キャリア開発賞を受賞したことで、大きな弾みをつけました。この助成金は、今後5年間、心不全のメカニズムの解明とバイオマーカーの開発に向けた研究に資金を提供します。スタンフォード大学での最初の数年間、レディ氏は研究資金として、小児心臓財団からの助成金やCVICUへの寄付など、民間からの資金に頼っていました。これらの初期の助成金や寄付金によって予備データを確立することができ、現在では、これらを活用して権威あるNIH助成金を獲得することに成功しています。「今の私の地位を支えてくれたのは、民間からの資金でした」と彼女は述べています。
レディ医師は、患者さんたちが新しい治療法に挑戦する意欲に感銘を受けていると言います。「私が診ている子どもたちやご家族は素晴らしいです」と彼女は言います。「彼らはこの病気を持って生まれ、一生この病気と共に生きていきます。彼らをケアできることは光栄であり、彼らの粘り強さが、最善の治療法を見つけようとする私の原動力となっています。」
この記事は2015年秋号に掲載されました。 ルシール・パッカード 子供向けニュース.